PRESSÃO DE VAPOR
A pressão de vapor é a pressão exercida por um vapor em equilíbrio com o sólido ou o líquido que o gera. Todos os líquidos tendem a evaporar-se mais ou menos rapidamente, dependendo do líquido em questão (para ser mais preciso, isto também se aplica aos sólidos, embora essa tendência seja praticamente nula na grande maioria dos casos).
Por razões práticas, e desde que não seja necessária uma grande precisão nos cálculos, pode estabelecer-se a seguinte igualdade: 1 atm = 1 bar = 100 kPa = 760 torr = 14,7 PSI

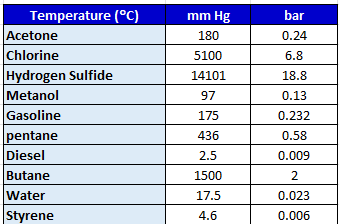
Na verdade, a pressão de vapor nada mais é do que uma indicação da capacidade de evaporação de uma substância. Os valores que podemos consultar em bases de dados ou fichas de segurança são proporcionais a essa capacidade; um valor elevado indica maior volatilidade do que um valor baixo. Para uma comparação rápida, podemos tomar como referência 100 mm Hg = 13,3 kPa = 0,13 bar. Uma substância cuja pressão de vapor esteja acima deste valor é altamente volátil; se não atingir 10 mm Hg, é muito pouco volátil; e se estiver acima de 500 mm Hg, a sua volatilidade é extrema. Se exceder 760 mm Hg, trata-se de uma substância gasos.
Dependendo da volatilidade do produto, a sua capacidade de dispersão será maior ou menor e determinará aspetos como as distâncias de intervenção, a deslocação do vapor para zonas mais baixas (dependendo da sua densidade em relação ao ar), a maior ou menor facilidade em tapar uma fuga e até a própria descontaminação, uma vez que, no caso de um produto muito volátil, poderá bastar expô-lo ao sol ou a uma zona bem ventilada.
.