FÓRMULA QUÍMICA E PESO MOLECULAR
Todas as substâncias puras podem ser representadas pela sua fórmula química, que constitui uma forma simples de refletir a sua composição molecular. As fórmulas químicas têm um duplo significado: qualitativo, que indica os diferentes átomos que compõem a molécula, e quantitativo, uma vez que também indica a proporção de cada um deles.
O peso molecular ou massa molecular relativa é a soma das massas atómicas de todos os átomos contidos numa molécula. Assim, por exemplo, sem ter em conta as casas decimais, a massa atómica do hidrogénio é 1; a do carbono é 12; a do azoto, 14; e a do oxigénio, 16. Portanto, a massa molecular do oxigénio (O2) será de 32; a do azoto (N2), 28; o da água (H2O), 18; o da amoníaca (NH3), 17; a estrutura do carbono (CO2), 44; and o do butano (C4H10), 58.
A fórmula indica-nos quais os elementos químicos que compõem uma substância. No caso da decomposição dessa substância, ou de uma reação com outra substância, podemos saber, ou pelo menos intuir, quais os novos produtos resultantes. Por exemplo, a combustão de um hidrocarboneto não produzirá óxidos de azoto nem outros compostos azotados, uma vez que o azoto não faz parte da sua composição. No entanto, a combustão de amoníaco ou de nitrocelulose irá emiti-los.
O peso molecular é especialmente interessante quando se trata de líquidos voláteis e gases, para determinar a sua capacidade de subir ou de se depositar em zonas mais baixas. Para tal, basta compará-lo com o peso molecular do ar seco, que é de 29. Assim, gases como o dióxido de carbono (peso molecular 44) ou o butano (peso molecular 58), sendo mais pesados que o ar, tenderão sempre a descer. Por outro lado, o metano (peso molecular 16) ou a amoníaca (peso molecular 17) dispersar-se-ão, subindo facilmente.
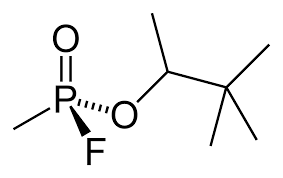 Soman
Soman
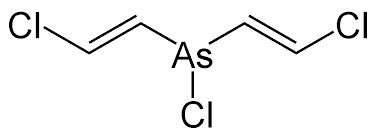 Lewisita
Lewisita
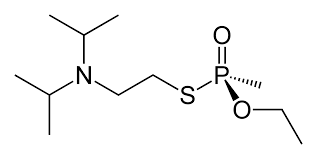 VX
VX
